20-21 лютого в м. Києві відбулася конференція PRO/PRE BIOTIC 2019, присвячена сучасним можливостям використання про- та пребіотичних препаратів в акушерстві й неонатології, при респіраторних захворюваннях, порушеннях імунітету, а також функціональних розладах шлунково кишкового тракту. Доповіді з питань пре- та пробіотичної терапії представили провідні українські фахівці, а також іноземні лікарі та вчені.
Запальні захворювання кишківника (ЗЗК): патогенез
Член правління Української гастроентерологічної асоціації, представник України у Європейському товаристві коліту та хвороби Крона, член Американської гастроентерологічної асоціації, член Товариства терапевтів України, доктор медичних наук, ппрофесор Андрій Едуардович Дорофєєв виступив з доповіддю «Роль кишкового мікробіому в розвитку запальних і функціональних захворювань кишечнику: можливості корекції».
– В Україні та загалом у світі зростає частота функціональних захворювань кишечнику (ЗК), тяжких форм хвороби Крона (ХК), неспецифічного виразкового коліту (НВК). Найімовірніше, ця тенденція в подальшому зберігатиметься. Зусилля науковців спрямовані на подолання зазначеної проблеми. Пацієнти з такою патологією потребують ретельної диференційної діагностики та тривалої терапії, адже, наприклад, тривалий перебіг НВК призводить до низки ускладнень, за яких необхідні важкі інвалідизуючі оперативні втручання.
У патогенезі запальних та функціональних ЗК значну роль відіграють зовнішнє середовище, імунологічний статус організму, стан мікробіому та генома.
На особливу увагу заслуговує генетичний фактор. Людина має розуміти, що її спосіб життя може вплинути на здоров’я її дітей та онуків. Одним з можливих пояснень збільшення частоти ХК і НВК в останні роки є виникнення поліморфізмів або мутацій упродовж життя та передача цих генетичних змін нащадкам. Реалізуючим фрагментом у розвитку переважно запальних ЗК є зміни регуляторних молекул цитокінів. Вивчення цих патогенетичних механізмів є важливим, оскільки отримані дані можна використати для розробки нових методів терапії.
Реалізація схильності до розвитку кишкового запалення може відбуватися також через патогенасоційовану систему, в якій безпосередня роль належить мікробіоті та її компонентам. Цей напрям нині теж активно вивчається з метою пояснення патогенетичних механізмів виникнення СПК.
До таких механізмів відносять: спадковість, порушення моторики, вісцеральну гіперчутливість, зміну бар’єрної функції кишківнику, порушення сприйняття вісцеральних подій центральною нервовою системою, психічну патологію, інфекції/запалення зміну кишкового мікробіому, харчову алергію/непереносимість.
Два роки тому були внесені певні зміни в Римські критерії IV і сьогодні функціональні ЗК розглядаються як стан з елементами запалення та зміною мікробіоти.
Патогенетичні фактори ЗК реалізуються за рахунок негативного впливу на слизовий бар’єр. Складовими слизового бар’єру кишечнику є епітелій товстої кишки, мікробіом і слиз, який містить метаболіти й активні молекули, що секретуються організмом-хазяїном та бактеріальною флорою.
Необхідно зазначити, що у хворих на НВК спостерігається не лише порушення слизоутворення, а й безпосередньо клітинне запалення. Таким чином відбувається розвиток крипт-абсцесів – накопичення імунокомпетентних клітин у крипті. Аналогічна тенденція має місце у пацієнтів із СПК. Крипт-абсцесів у разі цієї патології не буває, але відзначається помірно виражена поліморфноклітинна активність, переважно за рахунок лімфоцитів і макрофагів.
Використання PAS-реакції при обох патологіях дозволяє виявити активні нейтрофіли. У випадку НВК такий результат є маркером високої патологічної активності та свідчить про необхідність призначення більш агресивної терапії.
Скринінговим маркером патологічних змін слизового бар’єру кишківнику є синдром надлишкового бактеріального росту, для виявлення якого використовується водневий дихальний тест із лактулозою або глюкозою.
У пацієнтів із функціональними та запальними ЗК показники цього тесту практично однакові, що підкреслює однакову роль кишкової флори в обох випадках.
Мікробіом кишківника при ЗЗК
Механізм розвитку змін кишкового мікробіому досить складний. Важливу роль відіграють стан імунітету, дієта,
а також власне мікрофлора і її метаболічна та функціональна активність. Ми вивчали рівень мікроорганізмів родів Firmicutes, Bacteroides та Actinobacteria в пацієнтів із НВК та здорових осіб. У хворих на НВК було виявлено тенденцію до зниження колонізації Firmicutes та Bacteroides, передусім за рахунок збільшення популяції прото- й актинобактерій.
Також при НВП відзначалося зниження рівня біфідобактерій. Ключовим напрямом впливу на мікробіом та слизовий бар’єр кишечнику є пошук бактерій – «диригентів мікробіологічного оркестру». На сьогодні одним з найбільш перспективних варіантів такого пошуку є дослідження Faecalibacterum prausnitzii, оскільки ці мікроорганізми відповідають за активний синтез бутирату. До того ж вони не лише самі синтезують бутират, а й активно стимулюють його продукцію симбіотичною флорою.
Вплив на рівень бутирату важливий, оскільки ця сполука має протизапальні властивості, нормалізує стан слизового бар’єру кишечнику,а на клітинному рівні пригнічує синтез прозапальних цитокінів, зокрема фактора некрозу пухлини та інтерлейкінів 1 і 6.
Bifidobacterium infantis 35 624
Нещодавно на ринку України з’явився пробіотик, що містить штам Bifidobacterium infantis 35 624. Ця бактерія була виділена зі слизової оболонки термінального відділу тонкої кишки здорової людини. У доклінічних дослідженнях виявлені такі характеристики B. infantis 35 624, що дозволяють застосовувати її для корекції слизового бар’єру:
• відсутність передачі резистентності;
• здатність до виживання при транзиті через шлунково-кишковий тракт;
• стійкість до дії кислого середовища та жовчі;
• визначена чутливість до антибіотиків;
• підвищення резистентності до Salmonella;
Ефективність застосування B. infantis у пацієнтів із СПК також вивчали в клінічних дослідженнях. Так, P.J. Whorwell і співавт. (2006) провели дослідження за участю жінок (n=362) з діагнозом СПК, які протягом 4 тижнів отримували пробіотичний штам B. infantis 35 624.
Результати дослідження показали, що в пацієнток, які приймали пробіотик, відбувалося достовірне зниження больового синдрому порівняно з плацебо (рис.).
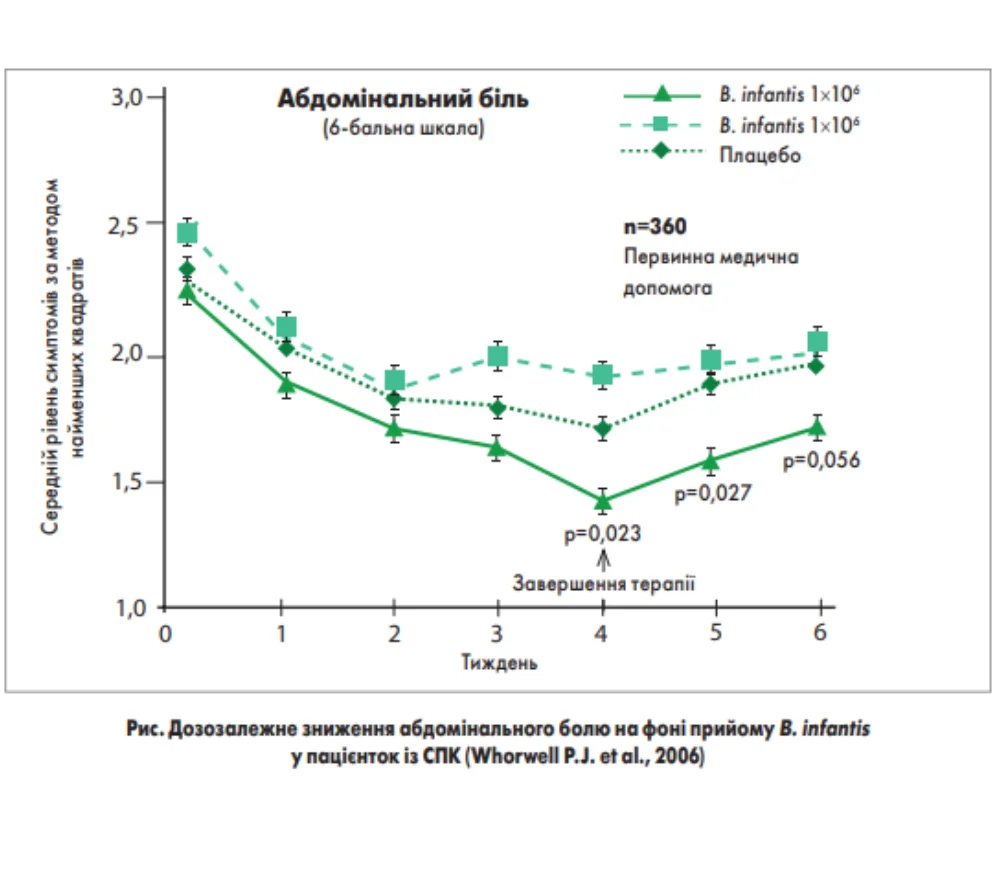
Автори зробили висновок, B. infantis здатен специфічно знижувати симптоми СПК. У дозуванні 1×108 B. infantis може призначатися в таблетованій формі, що підходить для широкого використання.
Отже, слизовий бар’єр є ключовою ланкою патогенезу ЗК. Перспективним напрямом терапії пацієнтів з функціональними та запальними ЗК є модулювання слизового бар’єру за допомогою ефективних пробіотиків. Такий пробіотичний штам, як B. infantis 35 624, довів свою ефективність у лікуванні пацієнтів із СПК.
Література:
- Тетяна Олійник та Ігор Кравченко; "Роль пробіотиків у лікуванні функціональних порушень шлунково-кишкового тракту"; Березень 2019; медична газета "Здоров'я України"; №5; Гастроентерологія; ст. 54-55;

